주기율표의 33 번째 원소는 비소이다. 그룹-15 의 요소는 비소이며 그 기호는’로’입니다. 비소는 원자가 전자를 통해 결합을 형성합니다. 이 기사에서는 비소의 원자가 전자에 대해 자세히 설명합니다. 바라건대,이 기사를 읽은 후 당신은 비소에 대해 자세히 알 수(으로)원자가 전자.
목차
비소는 얼마나 많은 전자와 양성자를 가지고 있습니까?
핵은 원자의 중심에 위치한다. 양성자와 중성자는 핵에 있습니다. 비소의 원자 번호(같이)는 33 입니다. 원자 번호는 양성자의 수입니다.
즉,비소의 양성자 수는 33 개입니다. 양성자와 동일한 전자는 핵 외부의 원형 껍질에 있습니다. 즉,비소 원자는 총 33 개의 전자를 가지고 있습니다.
비소의 원자가 전자는 무엇입니까?
비소의 전자 구성 후 마지막 껍질에있는 전자의 총 수를 비소의 원자가 전자라고합니다. 원자가 전자는 마지막 궤도(쉘)에있는 전자의 총 수입니다.

원자가 전자는 원소의 특성을 결정하고 결합 형성에 참여합니다. 주기율표에서 33 요소는 비소(으로). 즉,비소 원소의 원자는 총 33 개의 전자를 가지고 있습니다.
비소의 전자 구성은 비소의 마지막 껍질에 총 5 개의 전자가 있음을 보여줍니다. 즉,우리는 비소의 원자가 전자가 5 라고 쉽게 말할 수 있습니다. 이 사이트에는 비소의 전자 구성을 자세히 설명하는 기사가 있으며 원하는 경우 읽을 수 있습니다.
비소 원자의 원자가 전자의 수를 어떻게 계산합니까?
이제 우리는 비소의 원자가 전자를 쉽게 결정하는 방법을 알게 될 것입니다. 원자가 전자는 몇 가지 단계에 따라 결정되어야한다. 전자 구성이 그 중 하나입니다. 전자 구성없이 원자가 전자를 결정하는 것은 불가능합니다.
올바른 방법으로 전자 구성을 알면 모든 원소의 원자가 전자를 결정하는 것이 매우 쉽습니다. 전자 구성을 자세히이 사이트에 게시 된 기사가있다,당신이 원하는 경우에 당신은 그것을 읽을 수 있습니다. 그러나이 기사에서는 전자 구성에 대해 간략하게 설명합니다.
과학자 닐스 보어는 원자의 궤도(쉘)의 아이디어를 제공하는 첫번째이었다. 그는 1913 년에 원자 모델을 제공했습니다. 궤도의 완전한 아이디어는 거기에 주어진다. 원자의 전자는 특정 원형 경로에서 핵을 중심으로 회전합니다. 이러한 원형 경로를 궤도(쉘)라고합니다. 이 궤도는 엔.
케이 첫 번째 궤도(쉘)의 이름이고,엘 두 번째,미디엄 세 번째,엔 네 번째 껍질의 이름입니다. 각 궤도의 전자 보유 용량은 2 엔 2.
현재,
- 엔=1 케이 궤도.
케이 궤도의 전자 보유 용량은 2 엔 2=2,000,000,000,000=2 개의 전자이다.2834> - 에 대한 엘 궤도,엔=2.
전자 보유 용량 엘 궤도는 2 엔 2=2 22=8 전자.2834> - 엔=3 미디엄 궤도.
최대 전자 보유 용량 미디엄 궤도는 2 엔 2=2 22=18 전자.2834> - 엔=4 엔 궤도.
엔 궤도에서 최대 전자 보유 용량은 2 엔 2=2,000,000,000,000 42=32 전자이다.
이 방법 외에도 전자 구성은 하위 궤도를 통해 수행 할 수 있습니다. 독일의 물리학 자 아우프 바우는 먼저 하위 궤도를 통한 전자 구성에 대한 아이디어를 제안했습니다. 아우 바우 방법은 하위 에너지 레벨을 통해 전자 구성을 수행하는 것입니다.
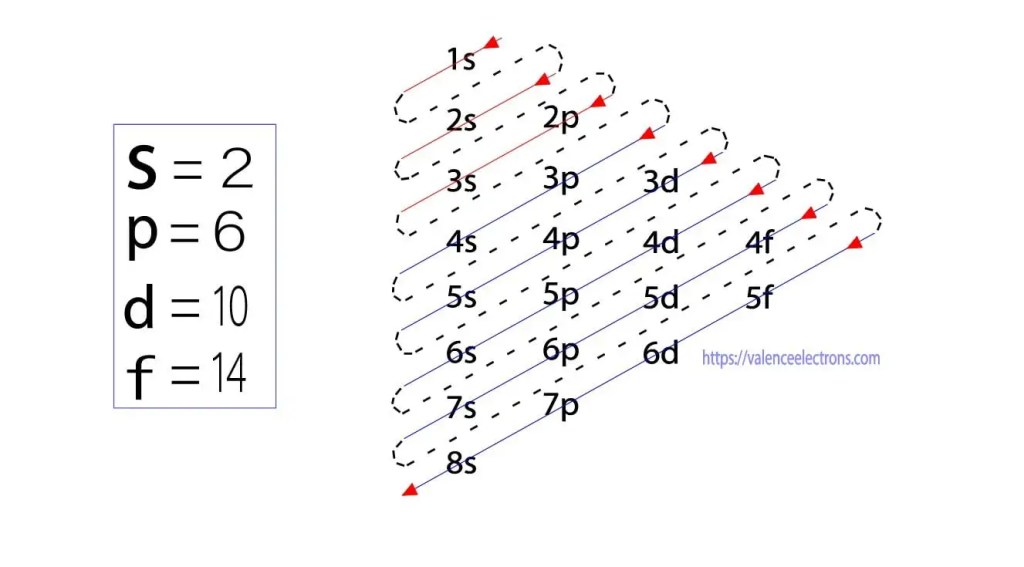
이 하위 궤도는’엘’으로 표현됩니다. 아우 바우의 원리는 원자에 존재하는 전자가 먼저 가장 낮은 에너지 궤도를 완성 한 다음 점차적으로 더 높은 에너지 궤도를 완성한다는 것입니다. 이 궤도의 전자 보유 용량은 에스=2,피=6,디=10 과 에프=14.
그러나,원자가 전자는 보어 원리에 따라 전자를 배열함으로써 쉽게 식별 될 수있다. 이제 우리는 비소의 원자가 전자를 결정하는 방법을 배울 것입니다.
1 단계:비소의 총 전자 수 결정(같이)
1 차 우리는 비소 원자의 총 전자 수를 알아야합니다. 전자 수를 알기 위해서는 비소의 양성자 수를 알아야합니다. 그리고 양성자의 수를 알기 위해서는 비소 원소의 원자 번호를 알아야합니다.
원자 번호를 알고 우리는 주기율표의 도움을 받아야한다. 이 비소의 원자 번호를 알 필요가있다(로)주기율표에서 요소. 원자 번호는 양성자의 수입니다. 그리고 양성자와 동일한 전자는 핵 외부에 위치합니다.

즉,우리는 마침내 비소 원자에 원자 번호와 동일한 전자가 있다고 말할 수 있습니다. 주기율표에서,우리는 비소의 원자 번호(로)33 것을 알 수있다. 즉,비소 원자는 총 33 개의 전자를 가지고 있습니다.
단계-2: 비소의 전자 구성을 할 필요가
단계-2 는 매우 중요합니다. 이 단계에서 비소의 전자를 배열 해야 합니다. 우리는 비소(원자)가 총 33 개의 전자를 가지고 있다는 것을 알고 있습니다. 비소의 전자 구성은 케이 껍질에 두 개의 전자,엘 껍질에 8 개,미디엄 껍질에 18 개,엔 쉘(궤도)에 5 개가 있음을 보여줍니다.

즉,비소의 첫 번째 껍질에는 두 개의 전자가 있고 두 번째 껍질에는 8 개의 전자가 있으며 세 번째 껍질에는 18 개의 전자가 있고 네 번째 껍질(마지막 궤도)에는 5 개의 전자가 있습니다. 비소 껍질 당 전자의 수는 2,8,18,5 입니다. 비소의 전자 구성은 하위 궤도를 통해 1 초 2 초 2 초 2 초 6 초 3 초 6 초 4 초 2 초 3 초 10 초 3 초 3 초.
단계-3: 원자가 쉘을 결정하고 총 전자를 계산
세 번째 단계는 원자가 쉘을 진단하는 것입니다. 전자 구성 후 마지막 껍질을 원자가 껍질(궤도)이라고합니다. 원자가 포탄에 있는 전자의 총계 수는 원자가 전자에게 불립니다. 비소의 전자 구성(같이)는 비소의 마지막 껍질에 5 개의 전자가 있음을 보여줍니다. 따라서 비소 원자는 5 개의 원자가 전자를 갖는다.
비소 이온(3-)은 얼마나 많은 원자가 전자를 가지고 있습니까?
마지막 껍질(궤도)에 5,6 또는 7 개의 전자를 가진 원소는 결합 형성 중에 마지막 껍질의 전자를 수신합니다. 전자를 받고 결합을 형성하는 요소를 음이온이라고합니다. 즉,비소(음이온)는 음이온 원소입니다.비소 결합이 형성되는 동안,마지막 껍질은 전자를 받아 비소 이온(비소 이온)으로 변한다. 비소 이온의 전자 구성은 다음과 같습니다.
비소 이온의 전자 구성은 비소 이온이 4 개의 쉘을 가지고 있고 마지막 쉘은 8 개의 전자(4 에스 2 4 피 6)를 가지고 있음을 보여줍니다. 전자 구성은 비소 원자가 크립톤의 전자 구성을 획득했음을 보여줍니다. 비소 이온의 마지막 껍질에는 8 개의 전자가 있기 때문에 비소 이온의 원자가 전자(3-)는 8 입니다.
비소의 원자가 란 무엇입니까?
원소의 한 원자가 분자를 형성하는 동안 다른 원자와 결합하는 능력을 원자가(원자가)라고합니다. 원소의 마지막 궤도에서 쌍을 이루지 않은 전자의 수는 그 원소의 원자가이다. 에 대한 전자 구성 비소(으로),우리는 5 개의 전자가 비소의 마지막 껍질에 존재한다는 것을 알 수 있습니다. 따라서 비소의 원자가(같이)는 5 입니다.

다시,원자가 여기 상태에서 요소의 전자 구성에서 결정 됩니다. 여기 상태에서 비소의 전자 구성은 다음과 같습니다. 여기서 비소의 전자 구성은 마지막 껍질에 세 개의 짝이없는 전자가 존재한다는 것을 보여줍니다. 이 경우 비소 원자의 원자가 3 입니다.
비소의 산화 상태는 결합 형성에 의존한다. 비소의 산화 상태는+3 입니다. 비소+3 의 산화 상태는 갈륨 비소에 사용되었습니다. 이 화합물의 비소 원자가는 3 입니다.