a periódusos rendszer 33.eleme az arzén. A 15. csoport eleme az arzén, szimbóluma pedig ‘As’. Az arzén kötéseket képez Valencia elektronjain keresztül. Ez a cikk részletesen tárgyalja az arzén vegyértékelektronjait. Remélhetőleg a cikk elolvasása után részletesen megismerheti az arzén (As) vegyérték elektronokat.
Tartalomjegyzék
- hány elektron és proton van az arzénban?
- melyek az arzén(As) vegyértékelektronjai?
- hogyan lehet kiszámítani a vegyérték elektronok számát egy arzénatomban?
- 1.lépés: az arzén(As) elektronok teljes számának meghatározása
- 2. lépés: Az arzén
- 3. lépés: A vegyértékhéj meghatározása és az összes elektron kiszámítása
- hány vegyértékelektronnal rendelkezik az arzénion (As3 -)?
- mi az arzén valenciája?
hány elektron és proton van az arzénban?
a mag az atom közepén helyezkedik el. A protonok és a neutronok az atommagban helyezkednek el. Az arzén(As) atomszáma 33. Az atomszám a protonok száma.
vagyis az arzénben lévő protonok száma harminchárom. A protonokkal egyenlő elektronok egy kör alakú héjban helyezkednek el a magon kívül. Vagyis egy arzén atomnak összesen harminchárom elektronja van.
melyek az arzén(As) vegyértékelektronjai?
az arzén elektronkonfigurációját követő utolsó héjban lévő elektronok teljes számát az arzén vegyértékelektronjainak nevezzük. A vegyérték elektron az utolsó pályán(héj) lévő elektronok teljes száma.

a vegyérték elektronok meghatározzák az elem tulajdonságait és részt vesznek a kötések kialakulásában. A periódusos rendszer 33. eleme az arzén (As). Vagyis az arzén elem atomjának összesen harminchárom elektronja van.
az arzén elektronkonfigurációja azt mutatja, hogy az arzén utolsó héjában összesen öt elektron van. Vagyis könnyen elmondhatjuk, hogy az arzén vegyértékelektronjai öt. Van egy cikk ezen az oldalon, amely részletezi az arzén elektronkonfigurációját, elolvashatja, ha akarja.
hogyan lehet kiszámítani a vegyérték elektronok számát egy arzénatomban?
most már tudjuk, hogyan lehet könnyen meghatározni az arzén vegyértékelektronjait. A vegyértékelektront néhány lépés követésével kell meghatározni. Az elektron konfiguráció az egyik. A vegyérték elektron meghatározása elektronkonfiguráció nélkül nem lehetséges.
az elektronkonfiguráció helyes ismeretében nagyon könnyű meghatározni az összes elem vegyértékelektronjait. Ezen a webhelyen megjelent egy cikk, amely részletezi az elektron konfigurációját, elolvashatja, ha akarja. Ez a cikk azonban röviden tárgyalja az elektron konfigurációját.
Niels Bohr tudós volt az első, aki ötletet adott az atom pályájáról(héj). 1913-ban bemutatta az atom modelljét. A pálya teljes elképzelését ott adják meg. Az atom elektronjai egy bizonyos kör alakú úton forognak a mag körül. Ezeket a kör alakú utakat orbitnak(héjnak) nevezzük.
K az első pálya(héj) neve, L a második, M A harmadik, N a negyedik héj neve. Az egyes pályák elektrontartó kapacitása 2n2.
most,
- n = 1 K pályára.
a K pálya elektrontartó képessége 2N2 = 2 db 12 = 2 elektron. - L pályára, n = 2.
az L pálya elektrontartó képessége 2N2 = 2 db 22 = 8 elektron. - n=3 Az M pályán.
a maximális elektrontartó kapacitás az M pályán 2N2 = 2 db 32 = 18 elektron. - n=4 az N pályán.
a maximális elektrontartó kapacitás N pályán 2N2 = 2 db 42-32 elektron.
ezen módszer mellett az elektronkonfiguráció alpályákon keresztül is elvégezhető. A német fizikus Aufbau először az elektronkonfiguráció ötletét javasolta alpályákon keresztül. Az Aufbau módszer az elektronkonfiguráció elvégzése az alenergia szintjén keresztül.
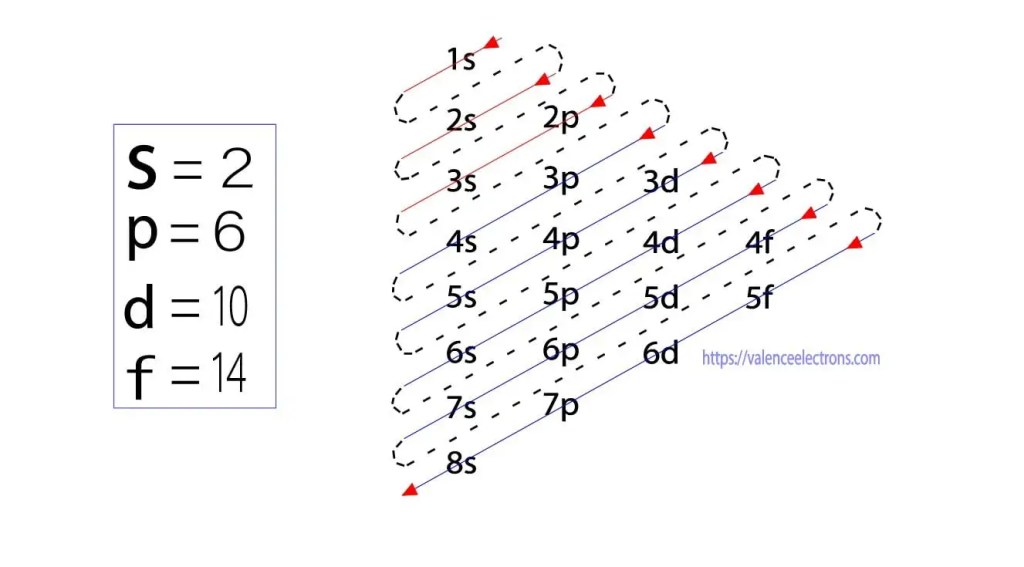
ezeket az alpályákat ‘ l ‘ fejezi ki. Az Aufbau-elv az, hogy az atomban jelen lévő elektronok először a legalacsonyabb energiájú pályát teljesítik, majd fokozatosan folytatják a magasabb energiájú pálya teljesítését. Ezen pályák elektrontartó képessége s = 2, p = 6, d = 10 és f = 14.
a vegyértékelektronok azonban könnyen azonosíthatók az elektronok Bohr-elv szerinti rendezésével. Most megtanuljuk, hogyan lehet meghatározni az arzén(As) vegyértékelektronját.
1.lépés: az arzén(As) elektronok teljes számának meghatározása
1. tudnunk kell az arzénatomban lévő elektronok teljes számát. Az elektronok számának megismeréséhez ismernie kell az arzénban lévő protonok számát. A protonok számának megismeréséhez ismernie kell az arzén elem atomszámát.
az atomszám megismeréséhez egy periódusos rendszer segítségét kell igénybe vennünk. Meg kell ismerni az arzén(As) elemek atomszámát a periódusos rendszerből. Az atomszám a protonok száma. A protonokkal egyenlő elektronok pedig a magon kívül helyezkednek el.

Vagyis végül elmondhatjuk, hogy az arzénatomban vannak olyan elektronok, amelyek megegyeznek az atomszámmal. A periódusos rendszerből azt látjuk, hogy az arzén(As) atomszáma 33. Vagyis az arzén atomnak összesen harminchárom elektronja van.
2. lépés: Az arzén
elektronkonfigurációjának elvégzése nagyon fontos a 2. lépés. Ebben a lépésben az arzén elektronjait el kell rendezni. Tudjuk, hogy az arzén(As) atomoknak összesen harminchárom elektronja van. Az arzén elektronkonfigurációja azt mutatja, hogy a K héjában két elektron van, nyolc az L héjában, tizennyolc az M héjában, öt pedig az N héjában(pálya).

vagyis az arzén első héjának két elektronja van, a második héjnak nyolc elektronja van, a 3.héjnak tizennyolc elektronja van, a 4. héjnak(utolsó pálya) pedig öt elektronja van. Az arzén(As) héjára jutó elektronok száma 2, 8, 18, 5. Az arzén elektronkonfigurációja az alpályán keresztül 1s2 2s2 2P6 3s2 3P6 4s2 3d10 4p3.
3. lépés: A vegyértékhéj meghatározása és az összes elektron kiszámítása
a harmadik lépés a vegyértékhéj diagnosztizálása. Az elektronkonfiguráció utáni utolsó héjat vegyértékhéjnak(orbit) nevezzük. A vegyértékű héjban lévő elektronok teljes számát vegyértékelektronnak nevezzük. Az arzén(As) elektronkonfigurációja azt mutatja, hogy az arzén utolsó héjának öt elektronja van. Ezért az arzénatomok 5 vegyértékelektronnal rendelkeznek.
hány vegyértékelektronnal rendelkezik az arzénion (As3 -)?
azok az elemek, amelyeknek 5, 6 vagy hét elektronja van az utolsó héjban(pályán), a kötésképződés során megkapják az utolsó héj elektronjait. Azokat az elemeket, amelyek elektronokat fogadnak és kötéseket képeznek, anionoknak nevezzük. Vagyis az arzén (As) anion elem.
As + 3e– AS3-
az arzénkötések kialakulása során az utolsó héj elektronokat fogad és arzénionokká alakítja(As3-). Az arzénionok elektronkonfigurációja(As3-) 1s2 2s2 2P6 3s2 3p6 4s2 3d10 4P6.
az arzénionok elektronkonfigurációja azt mutatja, hogy az arzénionoknak(As3-) négy héja van, az utolsó héjnak pedig nyolc elektronja van(4s2 4p6). Az elektronkonfiguráció azt mutatja, hogy az arzénatom megszerezte a Kripton elektronkonfigurációját. Mivel az arzénion utolsó héjának nyolc elektronja van, az arzénionok vegyértékelektronjai(As3-) nyolc.
mi az arzén valenciája?
az elem egyik atomjának azon képességét, hogy egy molekula képződése során csatlakozzon egy másik atomhoz, Valenciának (Valencia) nevezzük. A párosítatlan elektronok száma az elem utolsó pályáján az elem vegyértékessége. Az arzén(As) elektronkonfigurációjában azt látjuk, hogy öt elektron létezik az arzén utolsó héjában. Ezért az arzén(As) vegyértékértéke 5.

ismét a Valenciát az elem gerjesztett állapotban lévő elektronkonfigurációjából határozzuk meg. Az arzén elektronkonfigurációja gerjesztett állapotban*(33) = 1s2 2s2 2P6 3s2 3P6 4s2 3d10 4px1 4py1 4pz1. Itt az arzén elektronkonfigurációja azt mutatja, hogy három párosítatlan elektron létezik az utolsó héjban. Ebben az esetben az arzénatom valenciája 3.
az arzén oxidációs állapota a kötésképződéstől függ. Az arzén oxidációs állapota +3. Az arzén + 3 oxidációs állapotát Gallium-arzenidben (GaAs) alkalmazták. Az arzén vegyértéke ebben a vegyületben 3.